中国工程院院士、南开大学校长曹雪涛与第二军医大学医学免疫学国家重点实验室副教授顾炎、天津医科大学附属肿瘤医院教授付丽等合作,揭示了B细胞能通过分泌靶向肿瘤抗原HSPA4的病理性抗体,促进乳腺癌淋巴结转移。相关研究成果于1月15日在线发表在《自然-医学》杂志上。

早在2009年,曹雪涛院士团队就在J Immunol杂志上报道了利用新鲜分离出的小鼠肿瘤细胞与树突状细胞共培养,可以诱导其分化为调节性树突状细胞,抑制CD4+T细胞的增殖,从而提高肿瘤的免疫逃避。该项研究揭示了肿瘤微环境可以驯化非肿瘤细胞达到逃避免疫的目的。
2018年4月,曹雪涛院士团队曾在Cell杂志上发表文章,详细阐述了小鼠脾脏中被肿瘤诱导驯化的红系样细胞(erythroblast-like cells, or Ter-cells)可以释放artemin因子,促进肝癌的发展。利用抗体阻断artemin或其受体以及artemin敲除均可以抑制体内肝癌细胞的生长。在临床肝癌病人体内同样存在着可以分泌artemin的Ter-cell,血清中artemin含量升高与不良预后也呈现出强相关。该篇文章的报道进一步揭示了肿瘤驯化细胞在肿瘤发生和发展中的功能,为进一步寻找和研究其他肿瘤驯化细胞奠定了基础。
2019年1月在《自然-医学》杂志发表的这篇题为“Tumor-educated B cells selectively promote breast cancer lymph node metastasis by HSPA4-targeting IgG” 的最新研究中,研究团队利用小鼠乳腺癌原位模型,发现在肿瘤转移前,引流淋巴结中B细胞的比例与数量显著增加。并发现此类肿瘤驯化的B细胞可分泌大量抗体入血而促进乳腺癌淋巴结转移,实验性清除B细胞及其分泌的抗体,可以阻止乳腺癌淋巴结转移。
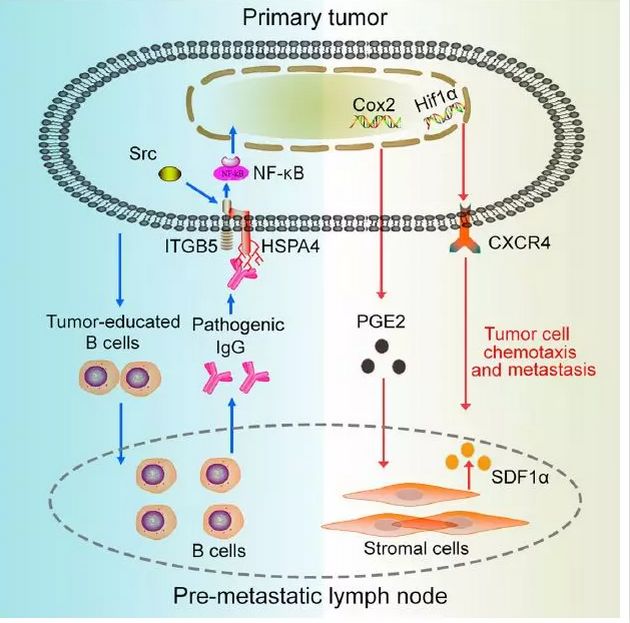
该研究阐明了B细胞及抗体介导的体液免疫在淋巴结转移前微环境形成及肿瘤淋巴结转移中的重要功能。此外,研究首次发现除调节性B细胞介导的负向免疫调控功能外,B细胞能够通过分泌靶向肿瘤抗原的病理性抗体直接促进肿瘤转移,同时寻找到糖基化的肿瘤膜抗原在病理性抗体的产生及促转移中的重要功能,为深入认识体B细胞介导的体液免疫功能及肿瘤转移前微环境的形成提供了新的视角,为肿瘤治疗尤其是肿瘤转移的预测和防治提供了新的靶点。














